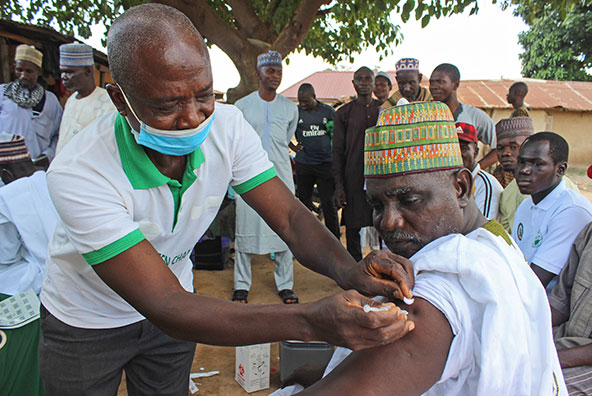
Une campagne de vaccination contre le coronavirus au Niger. Le pays affiche un taux de vaccination inférieur à 5 %. (Image: Keystone)
La « big pharma » – un terme désignant les grands groupes pharmaceutiques actifs dans la recherche et développement (R&D) – a livré plusieurs vaccins efficaces contre la Covid-19 avant fin 2020, lesquels étaient en partie financés par les gouvernements de certains pays riches. Ces lancements quasiment simultanés moins d’un an après la déclaration officielle d’une pandémie mondiale par l’Organisation mondiale de la santé (OMS) renforcent l’idée que le modèle commercial actuel de la R&D pharmaceutique est une poule aux œufs d’or qui sait pondre au moment opportun. Rien ne devrait donc venir le perturber.
Pourtant, près de deux ans après l’éclatement de la pandémie, une inégalité flagrante persiste : les pays à revenu élevé et intermédiaire supérieur ont utilisé environ trois quarts des doses de vaccin disponibles ; ceux à faible revenu n’en ont reçu que 4 %[1]. La société d’analyse scientifique Airfinity estime que le G7 et l’Union européenne (UE) disposeront d’un milliard de vaccins de plus que nécessaire d’ici fin 2021, dont 10 % devraient expirer cette année[2]. L’Afrique subsaharienne accuse notamment un important retard par rapport aux autres régions[3] : moins de 5 % de sa population devrait être entièrement vaccinée fin 2021. Cette inégalité amène à se demander si le modèle commercial des grands groupes pharmaceutiques est en panne.
Face à cette disparité, de pressants appels ont été lancés aux gouvernements pour qu’ils lèvent les droits de propriété intellectuelle (dérogation à l’accord sur les ADPIC[4]) dans le cadre de l’Organisation mondiale du commerce (OMC), ainsi qu’aux grandes entreprises pharmaceutiques pour qu’elles transfèrent « volontairement » et rapidement les technologies vaccinales à des sociétés compétentes en Afrique, en Amérique latine et en Asie. Les grands laboratoires estiment que le modèle actuel est adapté pour produire les doses de vaccin nécessaires d’ici début ou mi-2022. Selon eux, il appartient aux gouvernements des pays riches de payer les doses commandées à l’avance ou de les redistribuer aux régions dans le besoin.
Les modèles d’affaires de la « big pharma »
Les grands groupes pharmaceutiques doivent-ils appliquer un modèle de tarification basé sur les coûts et prévoyant des bénéfices raisonnables, mais non extraordinaires ? Ou doivent-ils s’en tenir au modèle fixant les prix en fonction de la valeur du nouveau médicament par rapport aux méthodes de traitement ou de prévention existantes ? Les organisations non gouvernementales (ONG) du domaine de la santé publique défendent le premier modèle. La « big pharma » est en revanche favorable à des médicaments protégés par la propriété intellectuelle, afin de pouvoir facturer le prix maximum que le marché est prêt à payer.
Fait surprenant, le format actuel n’a pas toujours prévalu. Au tournant de la Deuxième Guerre mondiale, les sociétés de R&D innovantes concédaient généralement leurs nouveaux produits sous licence à grande échelle, percevant des redevances raisonnables et sans bénéfices excessifs afin que les prix restent compétitifs. Cette situation avait plusieurs explications : premièrement, les médicaments innovants étaient moins nombreux ; deuxièmement, les brevets n’étaient ni demandés ni accordés aussi largement ; enfin, la réglementation n’était pas aussi stricte qu’aujourd’hui. Par conséquent, les dépenses de R&D et de marketing étaient beaucoup plus faibles.
À mesure que les brevets sur les médicaments devenaient la norme et que la réglementation des médicaments sur ordonnance se faisait plus stricte, les entreprises ont constaté que l’intégration en interne de la R&D et du marketing présentait un double avantage : d’une part, ces coûts essentiels étaient cachés au public ; d’autre part, le modèle du fournisseur unique – protégé par des brevets pour une durée moyenne de dix à douze ans – permettait de réaliser des bénéfices exceptionnels grâce à des prix fixés en fonction des capacités du marché et du caractère unique du nouveau médicament[5].
Un tollé général
Ce modèle s’est maintenu pendant des décennies sans être remis en question. Il a favorisé la mise au point de nombreux traitements préventifs et curatifs innovants – notamment contre le VIH, autrefois synonyme d’une mort certaine et désormais traité comme une maladie chronique à vie. Le triste sort de l’Afrique, où le Sida a fait des millions de morts et d’orphelins, a toutefois remis ce modèle en cause. Jusqu’au début des années 2000, le cocktail antirétroviral breveté pour traiter le VIH coûtait environ 15 000 dollars par patient et par an, un prix hors de portée pour la plupart des patients africains qui paient les médicaments de leur poche – comme dans la plupart des pays pauvres. Aujourd’hui, le même cocktail coûte moins de 100 dollars grâce aux versions génériques et au financement de donateurs.
Le lancement d’un traitement complet de l’hépatite C au prix exorbitant de 84 000 dollars par traitement, avait suscité la même indignation en 2013. Le laboratoire américain qui l’a développé a justifié son prix en avançant que le rapport qualité-prix était dans la norme des traitements précédents, notamment les greffes du foie pour les patients très atteints. Voyant que ce prix n’était pas abordable dans de nombreux pays pauvres, l’entreprise a proposé des remises et volontairement concédé une licence pour son médicament à plusieurs sociétés (notamment indiennes) moyennant une redevance de 7 %. Ces dernières ont ainsi pu approvisionner de nombreux autres pays à revenu faible ou intermédiaire[6].
Un secteur d’investissements à haut risque
Le problème de l’industrie pharmaceutique est qu’il s’agit d’un secteur à risques et investissements élevés qui, contrairement à d’autres, dépend uniquement des brevets et d’autres formes d’exclusivité pour valoriser ses dépenses de R&D[7]. L’octroi de licences à grande échelle et la tarification différenciée – même limités aux marchés des pays pauvres – font craindre le risque d’une fuite en avant. Ce phénomène explique sans doute que l’octroi volontaire de licences ou la vente à des prix inférieurs dans les pays à faible revenu ne soient pas plus courants dans l’industrie : celle-ci redoute que les pays riches réclament également des prix plus bas.
Certaines régions comme les États-Unis connaissent des hausses régulières des prix des médicaments sur ordonnance, car la surveillance réglementaire des prix y est faible. Cette pratique haussière est moins courante sur les marchés d’autres pays développés, où les prix des médicaments sont étroitement surveillés.
La solution généralement privilégiée serait d’instaurer un régulateur mondial bienveillant qui puisse gérer les prix des médicaments brevetés : le laboratoire de princeps obtiendrait ainsi un rendement optimal et incitatif de sa R&D et les coûts totaux de R&D seraient répartis raisonnablement sur le marché mondial. Le Fonds mondial de lutte contre le Sida, la tuberculose et le paludisme a proposé en 2013 un cadre mondial pour la tarification différenciée. Sa démarche a toutefois échoué face aux ONG du domaine de la santé publique, qui craignaient qu’elle ne limite l’usage des licences obligatoires et d’autres options autorisées par les ADPIC[8]. Faute d’un arbitre mondial de la tarification équitable, des anomalies persistent et voient les patients des pays pauvres payer parfois des prix bien plus élevés que ceux des pays riches.
En outre, l’industrie pharmaceutique n’est guère incitée à investir dans la R&D pour les maladies tropicales négligées, dont les victimes ont un très faible pouvoir d’achat. C’est pourquoi de nouveaux partenariats public-privé ont vu le jour afin de financer la R&D en faveur de nouveaux traitements prioritaires.
Certains experts du domaine de la santé[9] plaident depuis longtemps pour qu’un traité mondial sur la R&D dans le domaine médical soit négocié au sein de l’OMS et que tous les pays membres contribuent à un fonds commun en fonction de leur capacité de paiement. Ce fonds encouragerait la R&D portant sur de nouveaux traitements prioritaires dans le monde entier.
Même si l’industrie devrait accueillir favorablement des fonds supplémentaires pour la R&D en faveur des maladies négligées sans que cela perturbe leur modèle commercial actuel, la proposition visant à approfondir la question à l’OMS n’a pas avancé, sauf pour le financement volontaire de projets pilotes de R&D[10]. D’aucuns y voient en effet une tentative de changer le modèle actuel basé sur les droits de propriété intellectuelle. Au demeurant, peu de gouvernements semblent prêts à s’engager financièrement.
Quelles solutions d’avenir ?
Les divergences sur le modèle commercial des grands groupes pharmaceutiques persistent donc, même pour des médicaments et des vaccins destinés à traiter ou prévenir des maladies négligées et autres pandémies dans les pays pauvres. Les économistes considèrent la tarification différenciée ou échelonnée comme une solution profitable pour tous[11]. Un cadre mondial obligeant les grands laboratoires à pratiquer des prix proportionnés au revenu par habitant est nécessaire pour assurer sa mise en œuvre : il permettrait d’abaisser les prix dans les pays pauvres, tandis que les plus riches accepteraient de ne pas exiger les mêmes niveaux de prix.
Théoriquement, cette formule permettrait de résoudre la quadrature du cercle d’une répartition équitable des coûts de R&D pour des médicaments innovants. Aucun pays n’est cependant prêt à accepter aujourd’hui une hausse du prix des médicaments, tandis que les ONG du domaine de la santé publique craignent une dilution de l’accord ADPIC. Ce climat géopolitique ne laisse donc pas présager de consensus mondial concernant une révision prochaine du modèle commercial en vigueur.
- Our World in Data (2021). []
- Airfinity (2021). []
- Voir Pandem-ic (2021) pour des données actualisées sur la vaccination par régions. []
- Accord de l’OMC sur les Aspects des droits de propriété intellectuelle liés au commerce. Des négociations visant à suspendre certaines dispositions de cet accord en relation avec la pandémie de coronavirus ont actuellement lieu dans le cadre de l’OMC. Les développements ont été pris en compte jusqu’au délai de bouclage de la revue. []
- Voir Temin (1979, notamment p. 435–441) pour comprendre pourquoi le modèle commercial de R&D de la pharma a changé. []
- Voir Gilead (2015). []
- Cockburn (2009). []
- Saez (2014). []
- Voir Love et Hubbard (2007). []
- Third World Network (2016). []
- Danzon et Towse (2003). []
Bibliographie
- Airfinity (2021). More than 100 million vaccines are set to expire by the end of the year and need to be redistributed immediately. Communiqué de presse, 20 septembre.
- Cockburn I. (2009). « Intellectual property rights and pharmaceuticals : Challenges and opportunities for economic research ». Dans : Organisation mondiale de la propriété intellectuelle, The economics of intellectual property.
- Danzon P. et Towse A. (2003). « Differential pricing for pharmaceuticals : reconciling access, R&D and patents ». International Journal of Health Care Finance and Economics, vol. 3, 183–205.
- Gilead (2015). Chronic hepatitis c treatment expansion – Generic manufacturing for developing Countries. Février.
- Love J. et Hubbard T. (2007). « The big idea : Prizes to stimulate R&D for new medicines ». Chicago-Kent Law Review, vol. 82, 3.
- Our World in Data (2021). Covid-19 vaccine doses administered by country income group.
- Pandem-ic (2021). Global vaccination rates.
- Saez C. (2014). « Global Fund and tiered medicine pricing under debate ». TB Online, 7 avril.
- Temin P. (1979). « Technology, regulation, and market structure in the modern pharmaceutical Industry ». The Bell Journal of Economics, vol. 10, N° 2 (automne), 429–446.
- Third World Network (2016). « Members agree to postpone discussions on Medical R&D Treaty ». TWN Info Service on Health Issues, 16/01, 2 juin.
- OMS – Organisation mondiale de la santé (2012). Research and development to meet health needs in developing countries : strengthening global financing and coordination.
Bibliographie
- Airfinity (2021). More than 100 million vaccines are set to expire by the end of the year and need to be redistributed immediately. Communiqué de presse, 20 septembre.
- Cockburn I. (2009). « Intellectual property rights and pharmaceuticals : Challenges and opportunities for economic research ». Dans : Organisation mondiale de la propriété intellectuelle, The economics of intellectual property.
- Danzon P. et Towse A. (2003). « Differential pricing for pharmaceuticals : reconciling access, R&D and patents ». International Journal of Health Care Finance and Economics, vol. 3, 183–205.
- Gilead (2015). Chronic hepatitis c treatment expansion – Generic manufacturing for developing Countries. Février.
- Love J. et Hubbard T. (2007). « The big idea : Prizes to stimulate R&D for new medicines ». Chicago-Kent Law Review, vol. 82, 3.
- Our World in Data (2021). Covid-19 vaccine doses administered by country income group.
- Pandem-ic (2021). Global vaccination rates.
- Saez C. (2014). « Global Fund and tiered medicine pricing under debate ». TB Online, 7 avril.
- Temin P. (1979). « Technology, regulation, and market structure in the modern pharmaceutical Industry ». The Bell Journal of Economics, vol. 10, N° 2 (automne), 429–446.
- Third World Network (2016). « Members agree to postpone discussions on Medical R&D Treaty ». TWN Info Service on Health Issues, 16/01, 2 juin.
- OMS – Organisation mondiale de la santé (2012). Research and development to meet health needs in developing countries : strengthening global financing and coordination.
Proposition de citation: Watal, Jayashree (2021). Le modèle d’affaires des grands groupes pharmaceutiques est-il en panne ? La Vie économique, 29 novembre.









